RapidRead Technology

Technologie RapidRead
- L’intelligence artificielle (IA) fait indéniablement partie de notre quotidien. En tant que vétérinaires, nous avons la responsabilité de nous renseigner sur l’IA et sur l’impact qu’elle aura sur nos pratiques et les soins de nos patients.
- Cet article explique l’apprentissage automatique dans le contexte du diagnostic par imagerie vétérinaire et examine comment l’AIS occupe une position unique pour développer un produit d’IA solide et précis.
Article rédigé par Diane U. Wilson, DVM, DACVR (août 2023, mis à jour en mars 2024)
L’intelligence artificielle chez Antech Imaging Services
Apprentissage automatique
Dans les modèles (ou algorithmes) d’apprentissage automatique génératifs, la machine peut créer des solutions non programmées auparavant. Un exemple est le chatbot, ChatGPT, qui peut apprendre, créer et faire évoluer des conversations au fur et à mesure de son utilisation. Alors que, dans les modèles d’apprentissage automatique discriminants, la machine résout les informations uniquement en classifications pour lesquelles elle est programmée. Autrement dit, il identifie et catégorise uniquement ce pour quoi il a été initialement formé. Un modèle d’apprentissage discriminant ne peut pas évoluer vers quelque chose de plus. Actuellement, AIS utilise uniquement des modèles discriminants pour les techniques d’apprentissage automatique. (Figure 1)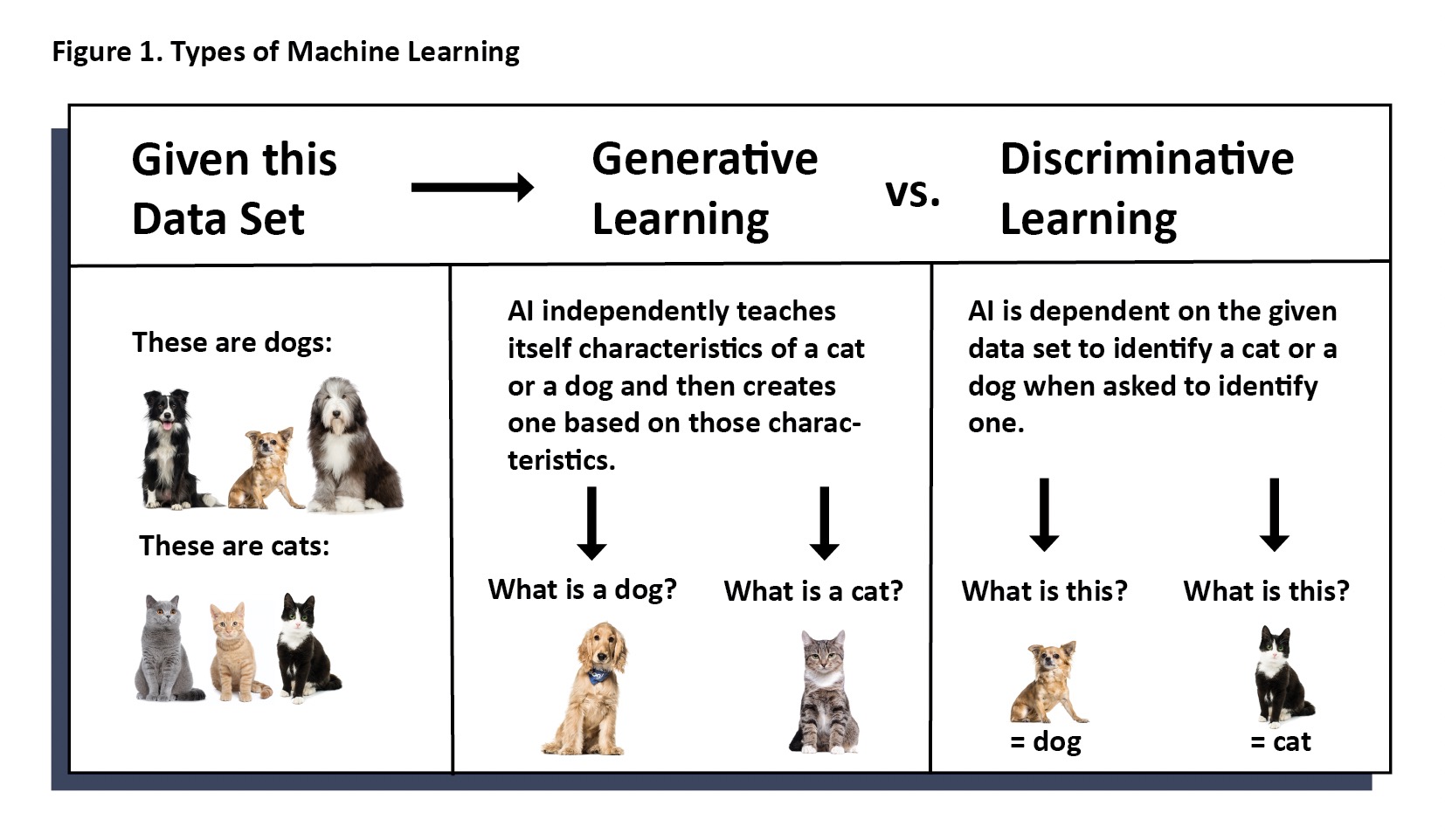
Que vous soyez optimiste ou pessimiste, l’IA est déjà largement utilisée en médecine vétérinaire. Comme dans d’autres domaines de la vie quotidienne, l’utilisation de l’intelligence artificielle peut être transparente pour l’utilisateur. Que l’utilisateur final soit un médecin généraliste, un technicien vétérinaire ou un spécialiste, il n’est pas évident que l’intelligence artificielle ait été utilisée, en tout ou en partie, pour atteindre un objectif. Parfois, l’IA est utilisée pour assister un autre programme dans le flux de travail ou pour aider un spécialiste à fournir des informations de diagnostic. Plus rarement, l’IA effectue un test de diagnostic complet sans intervention humaine.
L’intelligence artificielle est déjà présente en médecine vétérinaire
L’apprentissage automatique doit être effectué de manière responsable
 Des quantités massives de données sont nécessaires pour former un modèle sur chaque résultat. Sans données, nous ne pouvons pas affirmer de manière fiable des allégations d’exactitude, de sensibilité et de spécificité. Chez les humains, nous disons qu’une personne est experte dans un résultat d’imagerie particulier lorsqu’il existe une expérience d’au moins 500 cas de ce résultat. Malheureusement, il n’est pas possible pour une machine d’apprendre.
Des quantités massives de données sont nécessaires pour former un modèle sur chaque résultat. Sans données, nous ne pouvons pas affirmer de manière fiable des allégations d’exactitude, de sensibilité et de spécificité. Chez les humains, nous disons qu’une personne est experte dans un résultat d’imagerie particulier lorsqu’il existe une expérience d’au moins 500 cas de ce résultat. Malheureusement, il n’est pas possible pour une machine d’apprendre.
Chez AIS, nous avons déterminé que nous pouvons être sûrs du niveau mesuré d’exactitude, de sensibilité et de spécificité d’un modèle pour un résultat particulier, lorsque le modèle a rencontré quatre à cinq mille instances de ce résultat. Pour les résultats courants, comme un schéma bronchique pulmonaire, le nombre de cas nécessaire pour garantir l’exactitude peut être facile à acquérir. Pour les résultats moins courants tels que la discospondylarthrite, cela peut prendre plus de temps et nécessiter une collaboration entre plusieurs groupes pour obtenir le nombre de cas nécessaire pour entraîner le modèle en toute confiance.
 Des experts du domaine (spécialistes certifiés) sont nécessaires pour former et mesurer la précision de chaque modèle. Les radiologues (pathologistes, cardiologues, dentistes, etc.) passent des heures à étiqueter les images et à proposer des données corrigées à utiliser pour entraîner, évaluer et recycler la machine. De plus, il est nécessaire d’inclure une équipe d’experts du domaine pour qu’un consensus puisse être atteint, et la machine n’est pas formée sur l’opinion d’un seul individu. Des enquêtes tierces doivent être utilisées pour valider l’exactitude des cas connus.
Des experts du domaine (spécialistes certifiés) sont nécessaires pour former et mesurer la précision de chaque modèle. Les radiologues (pathologistes, cardiologues, dentistes, etc.) passent des heures à étiqueter les images et à proposer des données corrigées à utiliser pour entraîner, évaluer et recycler la machine. De plus, il est nécessaire d’inclure une équipe d’experts du domaine pour qu’un consensus puisse être atteint, et la machine n’est pas formée sur l’opinion d’un seul individu. Des enquêtes tierces doivent être utilisées pour valider l’exactitude des cas connus.
 Les data scientists constituent la base de l’équipe de programmation nécessaire au développement d’algorithmes de modèles. Les meilleures équipes comprennent des data scientists ayant une vision du produit, une solide collaboration avec des experts du domaine et une connaissance des besoins des utilisateurs finaux. Une équipe diversifiée avec des sous-spécialités uniques (segmentation, régression, analyse de données, divers logiciels) ainsi qu’une solide compréhension de tous les aspects de la science des données constituent une équipe des plus robustes, capable de surmonter les obstacles avec des solutions créatives.
Les data scientists constituent la base de l’équipe de programmation nécessaire au développement d’algorithmes de modèles. Les meilleures équipes comprennent des data scientists ayant une vision du produit, une solide collaboration avec des experts du domaine et une connaissance des besoins des utilisateurs finaux. Une équipe diversifiée avec des sous-spécialités uniques (segmentation, régression, analyse de données, divers logiciels) ainsi qu’une solide compréhension de tous les aspects de la science des données constituent une équipe des plus robustes, capable de surmonter les obstacles avec des solutions créatives.L’IA à l’AIS
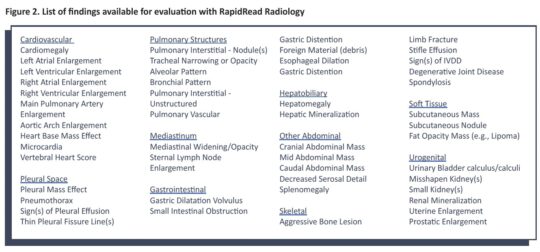
L’application clinique d’une liste de résultats signifie que plusieurs résultats différents peuvent être présents dans un rapport donné. Chaque résultat individuel peut avoir une précision d’au moins 95 % ; il faut toutefois tenir compte de la contribution globale du rapport en matière d’information à l’affaire.


D’autre part, RapidRead est largement formé aux résultats répertoriés dans la figure 2. Par exemple, si nous cherchons à savoir si un patient présente des modifications cardiaques ou pulmonaires qui pourraient contre-indiquer une anesthésie ou si nous cherchons à déterminer si un patient présentant des signes gastro-intestinaux est obstrué, alors RapidRead est un outil très utile pour accélérer les informations de niveau expert jusqu’au point de service. en quelques minutes (contre des heures ou des jours pour les lectures traditionnelles d’un radiologue).
Conclusion
Bibliographie
« Colossus : le projet Forbin ». Images universelles. 1970. Extrait de Prime Video.
Pu, Y., Apel, D.B. & Wei, C. Application des approches d’apprentissage automatique à l’évaluation de la responsabilité en matière de coups de toit : une comparaison des méthodes génératives et
Modèles discriminants.Application pure. Géophysique.176, 4503-4517 (2019). https://doi.org/10.1007/s00024-019-02197-1
Wilson, D.U., Bailey, M.Q., Craig, J. Le rôle de l’intelligence artificielle dans l’imagerie clinique et les flux de travail. VRUS. 63:S1, 897-902 (2022)
https://doi.org/10.1111/vru.13157
Fitzke, M, et. Al. OncoPetNet : un système d’IA basé sur l’apprentissage profond pour les figures mitotiques comptant sur H & E Images numériques de diapositives entières colorées
dans un grand laboratoire de diagnostic vétérinaire. Vidéo Youtube. https://www.youtube.com/watch?v=y_ZZUeW7Bvg&t=26s
Singh M, Nath G. Intelligence artificielle et anesthésie : une revue narrative. Saoudien J Anaesth. 2022 janvier-mars;16(1):86-93.
est ce que je: 10.4103/sja.sja_669_21. Publication en ligne le 4 janvier 2022. PMID : 35261595 ; PMCID : PMC8846233.
van Leeuwen, K.G., de Rooij, M., Schalekamp, S. et al.Comment l’intelligence artificielle en radiologie améliore-t-elle l’efficacité et les résultats en matière de santé ?.Pédiatre Radiol 52, 2087-2093 (2022).https://doi.org/10.1007/s00247-021-05114-8
Devant. Hum. Neurosci., 25 juin 2019 Sec. Neurosciences Sensorielles Volume 13 – 2019 |https://doi.org/10.3389/fnhum.2019.00213
Cohen, J, Fischetti, AJ, Daverio, H. Taux d’erreur radiologique vétérinaire déterminé par nécropsie. Échographie vétérinaire radiol. 2023 ; 1-12. DOI : 10.1111/vru.13259.

